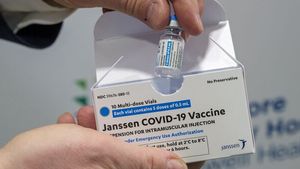
JAKARTA - Badan Pengawas Obat dan Makanan (FDA) Amerika Serikat pada Hari Senin menambahkan peringatan ke lembar fakta, untuk vaksin COVID-19 Johnson & Johnson, terkait dengan data adanya peningkatan risiko gangguan neurologis langka dalam enam minggu setelah vaksinasi.
Dalam sebuah surat kepada perusahaan, FDA mengklasifikasikan kemungkinan mendapatkan sindrom Guillain-Barré (GBS) setelah vaksinasi sebagai 'sangat rendah'.
Namun, dikatakan penerima vaksin Johnson & Johson (J&J) harus mencari pertolongan medis jika mereka memiliki gejala termasuk kelemahan atau sensasi kesemutan, kesulitan berjalan atau kesulitan dengan gerakan wajah, mengutip Reuters Selasa 13 Juli.
Sekitar 12,8 juta orang telah menerima vaksin satu dosis J&J di Amerika Serikat. FDA mengatakan, 100 laporan awal GBS pada penerima vaksin termasuk 95 kasus serius yang memerlukan rawat inap dan satu kematian yang dilaporkan.
Pihak J&J dalam sebuat pernyataan menyebut, mereka tengah berdiskusi dengan regulator tentang kasus GBS. Dikatakan, tingkat kasus GBS yang dilaporkan pada penerima vaksin COVID-19 J&J hanya sedikit melebihi tingkat latar belakang.
Untuk diketahui, peringatan ini pertama kali dilaporkan oleh Washington Post pada Hari Senin kemarin.

GBS adalah kondisi neurologis langka, di mana sistem kekebalan tubuh menyerang lapisan pelindung pada serabut saraf. Sebagian besar kasus mengikuti infeksi bakteri atau virus. kendati demikian, kebanyakan orang pulih sepenuhnya dari GBS.
Kondisi ini telah dikaitkan di masa lalu dengan vaksinasi, terutama dengan kampanye vaksinasi selama wabah flu babi di Amerika Serikat pada tahun 1976, dan beberapa dekade kemudian dengan vaksin yang digunakan selama pandemi flu H1N1 2009.
Sementara itu, Pusat Pengendalian dan Pencegahan Penyakit AS (CDC) dalam pernyataannya menyebut, sebagian besar kasus terjadi pada pria, banyak di antaranya berusia 50 tahun atau lebih. Tidak ditemukan kasus GBS yang lebih tinggi dari yang diperkirakan pada penerima vaksin berbasis mRNA dari Pfizer dan Moderna.
Pekan lalu, regulator European Medicines Agency (EMA) merekomendasikan peringatan serupa untuk suntikan COVID-19 AstraZeneca, yang didasarkan pada teknologi serupa dengan vaksin Johnson & Johnson.
BACA JUGA:
Peringatan tersebut merupakan kemunduran lain untuk suntikan J&J, yang seharusnya menjadi alat penting untuk memvaksinasi di daerah yang sulit dijangkau dan di antara mereka yang ragu untuk divaksinasi.
Sebab, vaksin ini hanya memerlukan satu suntikan dan memiliki persyaratan penyimpanan yang lebih longgar dibandingkan Pfizer atau moderna. Namun, sebelum ini vaksin J&J dikaitkan dengan pembekuan darah langka yang mengancam nyawa, serta masalah produksi di pabrik utama.
Kendati demikian, regulator AS memutuskan pada Bulan April lalu, manfaat vaksin melebihi risiko dari masalah pembekuan darah.