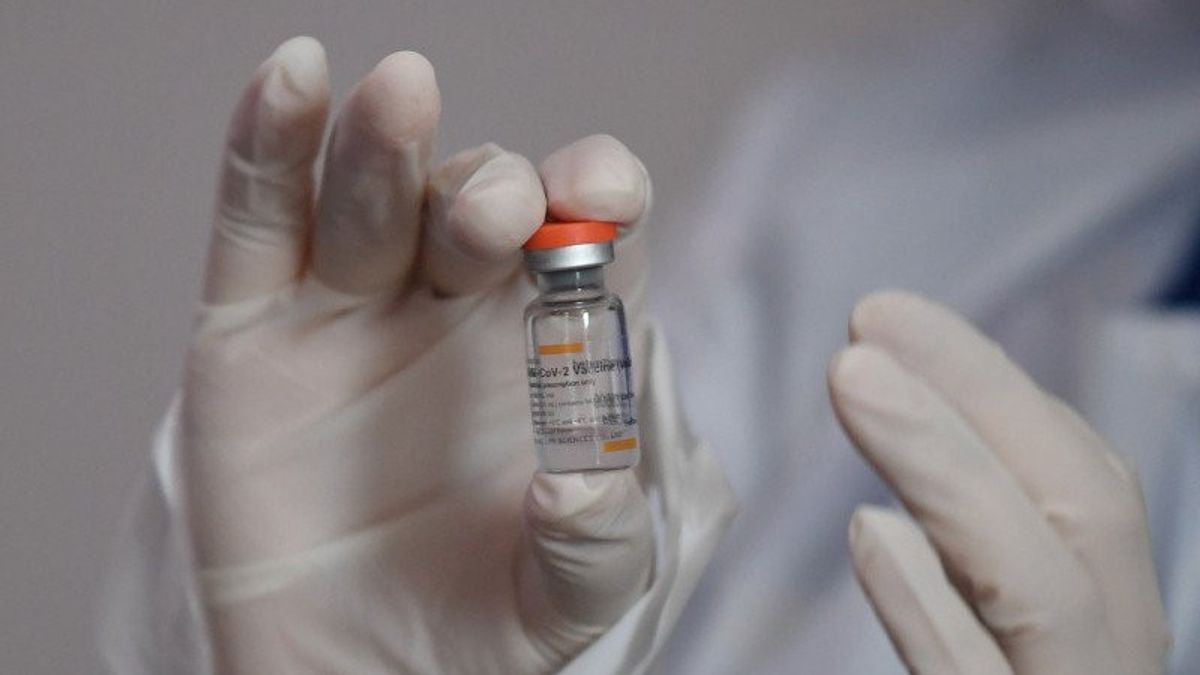
JAKARTA - Tim peneliti utama vaksin Nusantara, Kolonel Jhonny mengklaim pihaknya memiliki pengawas sendiri dalam menjalani pengembangan vaksin selain Badan Pengawas Obat dan Makanan (BPOM).
Namun, Jhonny enggan membeberkan lembaga mana yang mengawasi vaksin besutan mantan Menteri Kesehatan Terawan Agus Putranto tersebut.
"Kita, dalam pembuatan vaksin ini diaudit oleh suatu pihak ketiga untuk melihat good manufacturing product atau good manufacturing practice (GMP), jadi diawasi sesuai standar atau tidak," kata Jhonny di RSPAD Gatot Subroto, Jakarta Pusat, Rabu, 14 April.
"Pihak ketiganya siapa?" tanya wartawan.
"Satu badan yang melihat GMP. Dari siapanya masih rahasia," jawabnya.
Selain pengawas pihak ketiga, Jonny juga menyebut ada badan independen yang merupakan Organisasi Riset Kontrak (CRO) yang berbasis di Indonesia yang memberikan dukungan Uji Klinis berbasis Good Clinical Practice (GCP), yakni Prodia.
"Kemudian di dalam pelaksanaan uji klinis ini tahapan penelitiannya diawasi juga oleh badan independen juga, jadi kita dimonitoring,itu ada badannya, yaitu CRO clinical Research Organization, CRO ini kebetulan pada saat ini dari Prodia, jadi kita tidak bikin asal-asalan," tutur dia.
BACA JUGA:
Sebelumnya, Kepala Badan Pengawas Obat dan Makanan (BPOM) Penny K. Lukito membeberkan alasan pihaknya tidak memberi izin vaksin COVID-19 Nusantara untuk melakukan uji klinis fase II.
Penny bilang, tim peneliti vaksin besutan mantan Menteri Kesehatan Terawan Agus Putranto ini berulang kali mengabaikan hasil permintaan dan evaluasi BPOM.
Padahal, berdasarkan hasil uji klinis fase I oleh BPOM, vaksin Nusantara dinilai belum memenuhi banyak kaidah tahapan uji klinik, di antaranya good manufacturing practice dan good clinical practice.
“Komitmen correction action atau prevention action sudah diminta dari awal, tapi diabaikan, diabaikan, diabaikan. Tetap tidak bisa, nanti kembali lagi ke belakang. Jadi berbagai aspek, good clinical practice dan good manufacturing practice untuk produksi vaksin belum terpenuhi,” kata Penny.
Penny mengaku pihaknya belum meluluskan uji klinis fase I vaksin Nusantara, sehingga belum bisa mendapatkan persetujuan untuk fase II. Secara konsep, vaksin Nusantara juga belum valid dan data-data masih belum lengkap.