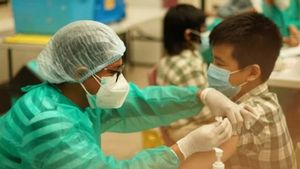
JAKARTA - Kepala Badan Pengawas Obat dan Makanan (BOPM) Penny K. Lukito menyebut pemerintah tidak melakukan uji klinis terhadap vaksin COVID-19 selain merek Sinovac yang akan digunakan di Indonesia.
Vaksin lain yang akan digunakan di Indonesia di antaranya AstraZeneca, China National Pharmaceutical Group Corporation (Sinopharm), Moderna, Novavax, Pfizer and BioNTech, dan yang diproduksi oleh PT Bio Farma yaitu vaksin Merah Putih.
"Untuk vaksin-vaksin lain yang akan dilakukan di Indonesia, tidak perlu ada uji klinis lebih jauh lagi," kata Penny dalam konferensi pers virtual, Jumat, 8 Januari.
Namun, BPOM akan tetap mengeluarkan izin kedaruratan atau emergency use authorization (EUA) terhadap vaksin lainnya. Namun, izin kedaruratan itu tidak memerlukan hasil uji klinis yang dilakukan oleh BUMN PT Bio Farma.
BACA JUGA:
Menurut Penny, BPOM cukup mendapatkan data izin kedaruratan dari sejumlah negara produsen vaksin yang telah melakukan uji klinis sendiri, seperti Amerika Serikat, Inggris, dan negara lain di Eropa.
"Dari EUA yang sudah diberikan negara-negara tersebut, kami hanya diberikan data yang lengkap, dikaitkan dalam proses pendaftaran mereka," tutur Penny.
"Itu adalah negara-negara yang sudah mendapatkan program reliance dengan Indonesia, sehingga ada aspek kepercayaan dan kecepatan dalam pemberian izin. Dalam waktu paling lama 20 hari kerja, akan segera keluar EUA-nya," lanjut dia.
Sebagai informasi, pemerintah mengamankan sekitar 400 juta dosis dari empat jenis vaksin COVID-19 dari berbagai negara. Ada 5 jalur pengadaan vaksin, yakni 4 dengan jalur bilateral dan 1 jalur multilateral.
Vaksin COVID-19 dari pengadaan bilateral meliputi Sinovac, Novavax, AstraZeneca, dan BioNTech Pfizer. Sementara, vaksin COVID-19 multilateral akan bekerja sama dengan organisasi vaksin internasional GAVI.