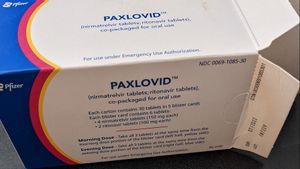
JAKARTA - Amerika Serikat (AS) pada hari Rabu mengesahkan pil antivirus COVID-19 lansiran Pfizer, untuk orang berusia 12 tahun ke atas yang berisiko sakit parah, menjadi pengobatan oral pertama di rumah sekaligus alat baru untuk melawan varian Omicron yang menyebar dengan cepat.
Rejimen antivirus Pfizer, Paxlovid, hampir 90 persen efektif dalam mencegah rawat inap dan kematian pada pasien dengan risiko tinggi penyakit parah, menurut data dari uji klinis perusahaan. Data laboratorium terbaru menunjukkan, obat tersebut tetap efektif melawan Omicron, kata Pfizer.
Pfizer menaikkan proyeksi produksi 2022 menjadi 120 juta program pengobatan dari 80 juta, mengatakan siap untuk memulai pengiriman segera di Amerika Serikat. Rejimen dua obat pengobatan termasuk obat baru dan antivirus kedua yang lebih tua yang disebut ritonavir.
Pemerintah AS akan memiliki 265.000 kursus perawatan yang tersedia pada Januari dan pasokan akan meningkat di bulan-bulan berikutnya, koordinator respons COVID-19 Gedung Putih Jeff Zients mengatakan pada sebuah pengarahan. Pemerintah mengharapkan untuk menerima 10 juta kursus yang telah dipesan dalam waktu enam bulan.
"Persetujuan Paxlovid adalah tonggak utama yang menandai langkah lain untuk menjadikan COVID-19 sebagai infeksi yang jauh lebih mudah dikelola," terang Amesh Adalja, seorang sarjana senior di Johns Hopkins Institute for Health Security, mengutip Reuters 23 Desember.
"Namun, ada dua masalah utama yang tersisa: Ini akan langka dalam beberapa minggu mendatang dan penggunaan optimalnya memerlukan diagnosis yang cepat, yang bisa jadi sulit dengan masalah pengujian terus-menerus yang mengganggu kami," tambah Adalja.
Terpisah, Pfizer mengatakan memiliki 180.000 kursus perawatan yang siap dikirimkan tahun ini. Kontrak pemerintah AS untuk 10 juta kursus obat dihargai 530 dolar AS per kursus.
Keputusan Administrasi Makanan dan Obat-obatan (FDA) untuk mengeluarkan otorisasi darurat perawatan ini datang ketika AS memerangi lonjakan kasus COVID-19 yang didorong oleh varian Omicron, dengan Presiden Joe Biden mengumumkan rencana untuk lebih banyak vaksinasi dan situs pengujian federal.
Pil dapat mengisi celah pengobatan yang dibuka oleh varian Omicron, kata William Schaffner, ahli penyakit menular terkemuka dari Vanderbilt University School of Medicine. Perawatan antibodi monoklonal yang paling banyak digunakan untuk COVID-19 terbukti kurang efektif dalam memerangi varian dan ada persediaan terbatas dari satu perawatan tersisa yang berfungsi, katanya.

Antibodi monoklonal biasanya diberikan secara intravena di rumah sakit, tidak tersedia secara luas dan lebih dari dua kali harga pil Pfizer.
Sementara itu, FDA mengatakan pihaknya mengizinkan Paxlovid untuk penggunaan darurat untuk pengobatan penyakit ringan hingga sedang pada orang dewasa dan anak-anak berusia 12 tahun ke atas, yang berisiko tinggi untuk berkembang menjadi COVID-19 yang parah.
Obat ini hanya tersedia dengan resep dokter dan harus dimulai sesegera mungkin setelah diagnosis COVID-19 dan dalam waktu lima hari setelah timbulnya gejala, sebut FDA. Pil dimaksudkan untuk diminum setiap 12 jam selama lima hari.
Sementara uji klinis tidak termasuk pasien di bawah usia 18 tahun, kata Pfizer, rejimen dosis orang dewasa yang berwenang diharapkan menghasilkan tingkat konsentrasi obat yang sebanding dalam darah pada pasien anak 12 dan lebih tua dengan berat setidaknya 40 kg (88,2 lbs).
Obat kedua, ritonavir, diketahui berinteraksi dengan beberapa obat resep lainnya. Pfizer mengatakan bahwa itu harus dapat dikelola dan menyarankan sebagian besar pasien akan dapat menurunkan dosis obat mereka yang lain saat dirawat untuk COVID-19.
BACA JUGA:
Pfizer mengatakan pihaknya berencana untuk mengajukan aplikasi obat baru dengan FDA pada tahun 2022 mencari persetujuan peraturan penuh.
Untuk diketahui, Pfizer telah setuju untuk mengizinkan produsen generik untuk memasok versi pengobatan ke 95 negara berpenghasilan rendah dan menengah melalui perjanjian lisensi dengan kelompok kesehatan masyarakat internasional, Medicines Patent Pool (MPP).
Pil saingan dari Merck & Co (MRK.N) sedang ditinjau oleh FDA. Obat, molnupiravir, yang dikembangkan dengan Ridgeback Biotherapeutics, mengurangi risiko rawat inap dan kematian sebesar 30 persen dalam uji coba.