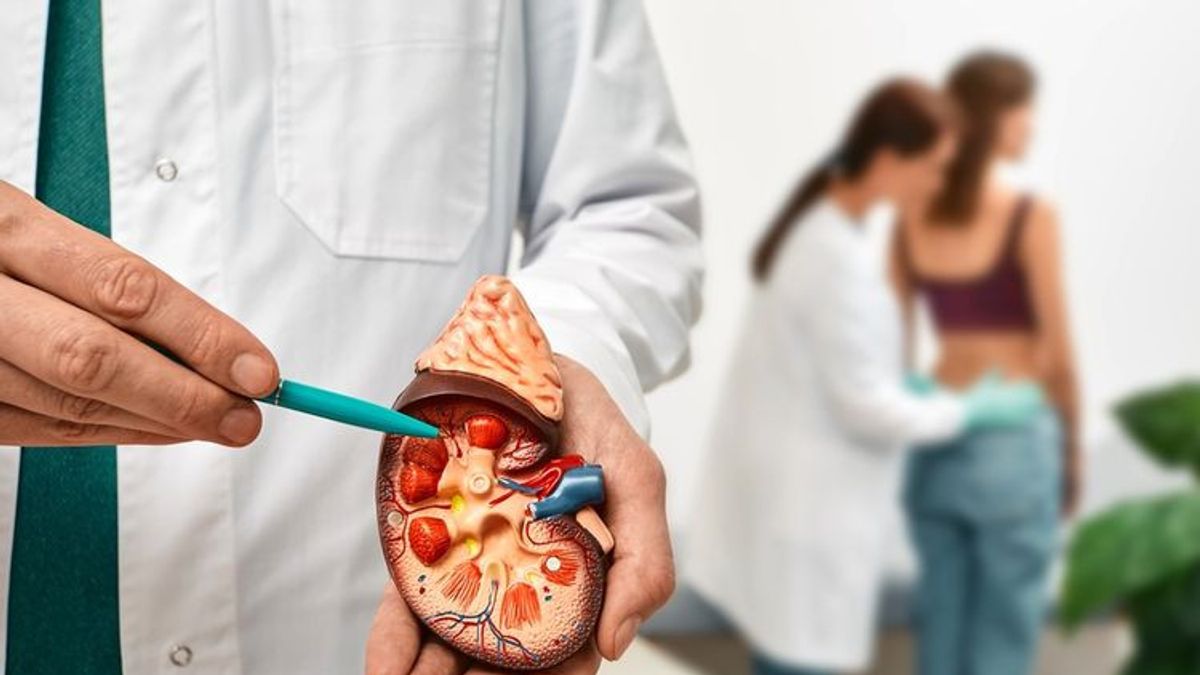
JAKARTA - Kementerian Kesehatan kembali memperbaharui kebijakannya terkait larangan penggunaan obat-obatan sirop sebagai langkah antisipasi bertambahnya jumlah pasien gangguan ginjal akut. Ini menyusul hasil pengujian oleh Badan Pengawasan Obat dan Makanan (BPOM).
Sejauh ini, 156 obat sirop dinyatakan aman tanpa zat tambahan.
“Tidak menggunakan propilen glikol, polietilen glikol, sorbitol, dan atau gliserin/gliserol, aman sepanjang digunakan sesuai aturan pakai,” kata Juru Bicara Kementerian Kesehatan dr. M Syahril dalam siaran pers, Selasa (25/10).
Dari jumlah tersebut, terdapat 23 obat hasil penelusuran Kemenkes di rumah pasien, yakni:
- Alerfed Syrup (Guardian Pharmatama)
- Amoxan (Sanbe farma)
- Amoxicilin (Mersifarma TM)
- Azithromycin Syrup (Natura/Quantum Labs)
- Cazetin (Ifras Pharmaceutical Laboratories)
- Cefacef Syrup (Caprifarmindo Labs)
- Cefspan syrup (Kalbe Farma)
- Cetirizin (Novapharin)
- Devosix drop 15 ml (Ifras Pharmaceutical Laboratories)
- Domperidon Sirop (Afi Farma)
- Etamox syrup (Errita Pharma)
- Interzinc (Interbat)
- Nytex (Pharos)
- Omemox (Mutiara Mukti Farma)
- Rhinos Neo drop (Dexa Medica)
- Vestein (Erdostein) (Kalbe)
- Yusimox (Ifras Pharmaceutical Laboratories)
- Zinc Syrup (Afi Farma)
- Zincpro syrup (Hexpharm Jaya)
- Zibramax (Guardian Pharmatama)
- Renalyte (Pratapa Nirmala)
- Amoksisilin (-)
- Eritromisin (-)
“Obat-obat ini dapat diresepkan kembali, termasuk 133 obat lainnya sesuai dengan rekomendasi BPOM,” ucap Syahril.



Selain itu, BPOM juga menemukan 3 obat sirop mengandung etilen glikol dan dietilen glikol melebihi ambang batas aman. Kepala BPOM Penny K. Lukito menduga cemaran etilen glikol dan dietilen glikol berasal dari penggunaan pelarut propilen glikol, polietilen glikol, sorbitol, dan gliserin/gliserol.
"Penggunaan pelarut memang tidak dilarang selama proses produksi terjaga baik. Selama ada di batas minimal, bisa ditolerir, maka dianggap aman. Tentu harus sesuai juga cara penggunaan obat, dosis, dan lamanya penggunaan obat tersebut," jelas Penny dalam Konferensi Pers di Kantor BPOM pada 23 Oktober 2022.
Ketiga obat tersebut, yakni:
- Unibebi Cough Sirop (Universal Pharmaceutical Industries)
- Unibebi Demam Drops (Universal Pharmaceutical Industries)
- Unibebi Demam Sirop (Universal Pharmaceutical Industries).
Sesuai acuan Farmakope dan standar baku nasional yang diakui, ambang batas aman atau Tolerable Daily Intake (TDI) untuk cemaran etilen glikol dan dietilen glikol sebesar 0,5 mg/kg berat badan per hari.
Namun, kata Guru Besar Famakokimia ITB Prof. Rahmana Emran Kartasasmita, melewati ambang keamanan tidak dimaknai keracunan, melainkan berisiko mengalami gangguan kesehatan.
“Sehingga perlu ada analisis lebih mendalam terkait itu,” ucapnya pada kesempatan sama.
BPOM akan terus melakukan pengawasan. Penny juga mengimbau masyarakat lebih waspada. Belilah obat di apotek, toko obat berizin, puskesmas, atau rumah sakit. Jangan di tempat-tempat sembarang.
“Kami juga mendorong tenaga kesehatan dan industri farmasi secara aktif melaporkan efek samping obat kepada Pusat Farmakovigilans/MESO Nasional melalui aplikasi e-MESO Mobile,” imbuh Kepala BPOM.
Penelitian Lebih Lanjut
Pengamat Farmasi, Anthony Charles Sunarjo menganggap apa yang dilakukan Kemenkes dan BPOM mengambil tindakan darurat dengan melarang penggunaan obat-obatan sirop sudah tepat.
Namun, lebih ideal lagi bila penelitian terus dilakukan untuk menemukan penyebab utama gangguan ginjal akut yang mayoritas menyerang balita.
“Saat ini kan masih dugaan sementara. Lagi pula kenapa baru sekarang terjadi outbreak, padahal sudah belasan bahkan puluhan tahun, mereka pakai obat-obatan tersebut. Kok bisa menimbulkan gagal ginjal akut?,” ujar mantan ketua GP Farmasi Indonesia tersebut kepada VOI, Selasa (25/10).
Lalu terkait dengan tiga obat temuan BPOM, Anthony pun mempertanyakan apakah seluruh pasien gangguan ginjal akut, baik yang sudah meninggal atau yang masih dirawat menggunakan ketiga obat tersebut.
“Logika sederhana saja, jadi kesimpulan saya butuh penelitian lebih lanjut. Jangan semata di obat-obatan saja, tetapi juga faktor-faktor lain, sehingga bila terjadi kasus seperti ini lagi, kita bisa lebih mudah mengatasinya,” katanya.

Memang, lanjut Anthony, kemungkinan ‘cacat’ dalam proses produksi obat bisa saja terjadi, tetapi sangat kecil. Sebab, proses produksi dalam industri obat-obatan di Indonesia sangat ketat.
“Kalau dilihat dari regulasi yang ada, istilahnya industri farmasi susah bernapas, karena memang penuh aturan. Mulai dari produsen, distribusi, sampai ke pelayanan apotek dan toko obat ada standar khusus yang sudah ditentukan dalam regulasi,” ucap Anthony.
Contoh proses produksi. Pembelian bahan baku harus disertai certicifate of analysis dari produsen. Saat pesanan datang, harus ditaruh di ruang sementara terlebih dahulu quality control dan mengambil sampel untuk cek laboratotrium.
“Setelah sesuai spesifikasi pabrik termasuk impurity check, barang masuk ke gudang permanen. Kemudian dilakukan quality control kembali. Barulah dikeluarkan ke gudang barang jadi untuk produksi. Ini disebut in process control,” Anthony menjelaskan.
Tak hanya itu, setiap pabrik obat juga harus memiliki retain sample sehingga bila ada sesuatu kemudian hari, obat bisa diteliti kembali melalui sampel yang ada.
Alhasil, kalau memang ada cemaran, kemungkinan terjadi di supply bahan baku pembantu atau yang disebut bahan larutan. Bukan di bahan baku utama.
“Barangkali ada perubahan supplier karena dampak pandemi pembatasan arus keluar masuk orang dan barang di sejumlah negara produsen obat-obatan, seperti di China dan India,” Anthony menduga.
“Biasanya kan tetap dengan sertifikat yang sama. Bila barang dapat dari supplier lain, ya berarti harus mulai dari nol lagi pengecekannya. Barangkali impurity checknya yang terlewat,” tambahnya.
BACA JUGA:
Menurut dr. M Syahril, sudah ada 255 kasus gangguan ginjal akut di Indonesia per 22 Oktober 2022 yang berasal dari 26 provinsi, 143 di antaranya meninggal dunia.
"Sejauh ini, larangan penggunaan, penjualan, dan larangan memberikan resep obat-obatan sirop sementara telah berhasil mencegah penambahan kasus baru di RSCM sebagai rumah sakit nasional rujukan gagal ginjal. Tidak ada penambahan kasus baru sejak 22 Oktober 2022," tandas Juru Bicara Kementerian Kesehatan tersebut.