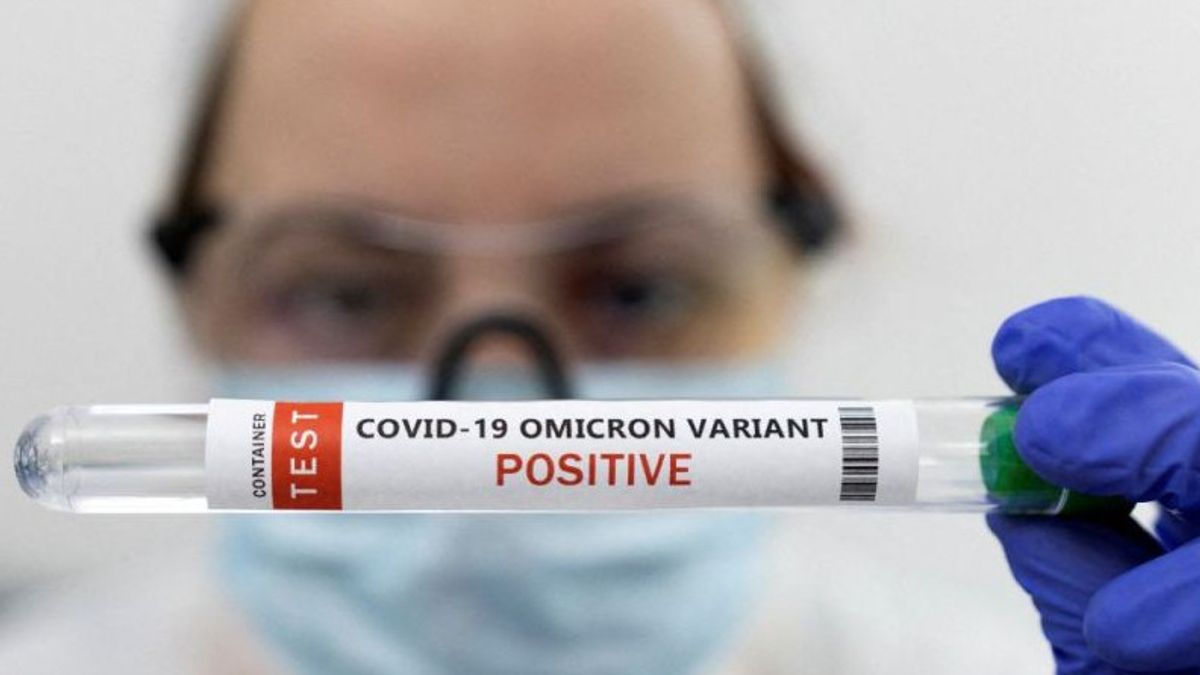
JAKARTA - Badan Pengawas Obat dan Makanan AS (FDA) untuk pertama kalinya menerbitkan izin penggunaan darurat diagnostik COVID-19 lewat sampel napas. Caranya adalah dengan menggunakan InspectIR COVID-19 Breathalyzer.
Melalui alat tersebut, tes dapat berlangsung di lingkungan tempat spesimen pasien terkumpul dan dianalisis, seperti kantor dokter, rumah sakit dan lokasi tes mobile, menggunakan instrumen seukuran barang bawaan.
"Tes dilakukan oleh operator berkualitas dan terlatih di bawah pengawasan penyedia layanan kesehatan berlisensi atau yang disahkan oleh undang-undang negara bagian untuk meresepkan tes dan dapat menyediakan hasilnya kurang dari tiga menit," kata FDA lewat pernyataan dikutip Antara, Jumat 15 April.
BACA JUGA:
Direktur Pusat Perangkat dan Kesehatan Radiologi (CDRH) FDA Jeff Shuren mengatakan izin tersebut merupakan contoh lain dari inovasi cepat yang terjadi dengan tes diagnostik untuk COVID-19.
"FDA terus mendukung pengembangan tes COVID-19 baru dengan tujuan meningkatkan teknologi yang dapat membantu mengatasi pandemi saat ini sekaligus memosisikan AS dengan lebih baik untuk menghadapi kedaruratan kesehatan masyarakat umum selanjutnya," katanya.
InspectIR COVID-19 Breathalyzer menggunakan teknik yang disebut kromatografi gas-spektrometri massa (GC-MS) untuk memisahkan serta mengidentifikasi campuran kimia.