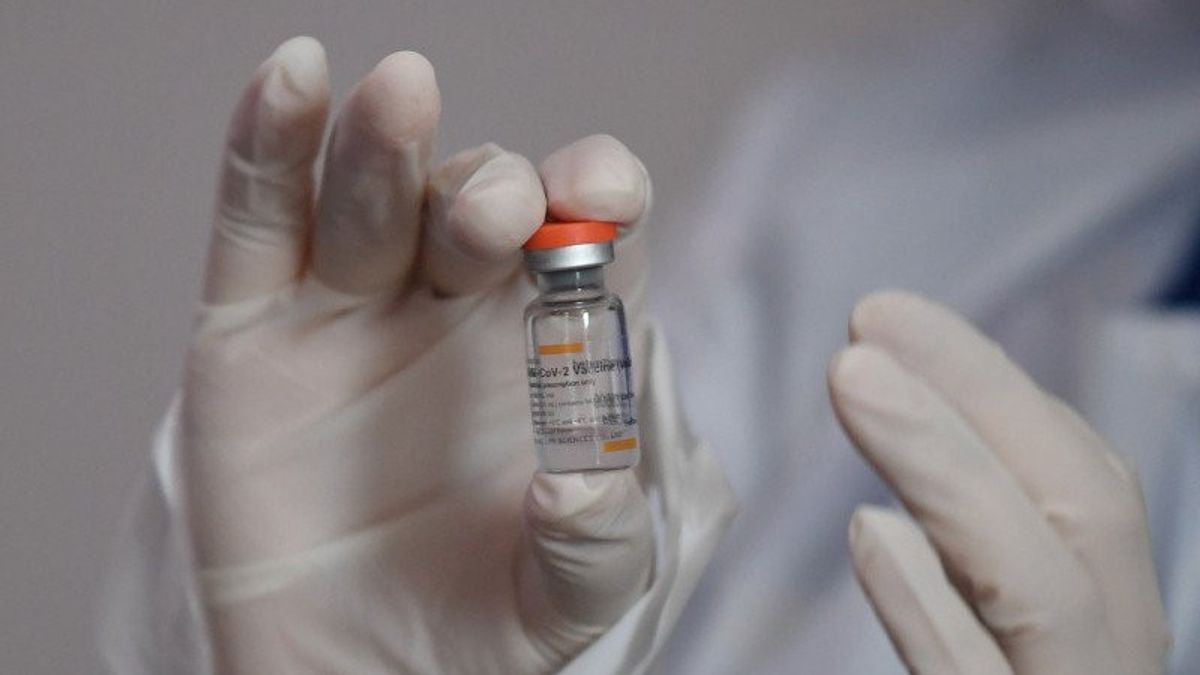
雅加达-努桑塔拉疫苗的主要研究小组,Jhonny上校声称,除了食品和药物管理局(BPOM)之外,它还有自己的疫苗开发主管。
然而,乔尼不愿透露由前卫生部长特拉万·阿古斯·普特兰托监督疫苗的机构。
4月14日,星期三,雅加达市中心Gatot Subroto医院的Jhonny说:"我们,在生产这种疫苗时,由第三方审核,以看到良好的制造产品或良好的制造实践(GMP),无论是否按标准进行监督。
"谁的第三方?
"一个看到GMP的身体。从谁,这仍然是一个秘密,"他回答。
除了第三方主管外,Jonny还提到,在印度尼西亚有一个独立的机构,是一个合同研究组织(CRO),根据良好的临床实践(GCP)提供临床试验支持,即Prodia。
他说:「在实施这项临床试验时,研究阶段亦由独立机构监管,因此我们受到监察,有一个机构,即CRO临床研究组织,CRO在这个时候是巧合,来自普罗迪亚,所以我们不作任何起源。
此前,美国食品和药物管理局(BPOM)局长Penny K. Lukito解释了为什么它没有允许COVID-19努桑塔拉疫苗进行II期临床试验。
佩妮说,疫苗研究小组由前卫生部长特拉万·阿古斯·普特兰托反复无视结果的要求和评价。
事实上,根据BPM第一阶段临床试验的结果,Nusantara疫苗被认为没有达到许多临床试验阶段的规则,包括良好的制造实践和良好的临床实践。
"承诺更正行动或预防行动从一开始就被要求采取,但被忽视、忽视、忽视。还是不能,背靠背。因此,疫苗生产的各个方面、良好的临床实践和良好的制造实践都没有得到满足,"Penny 说。
Penny承认,它尚未通过努桑塔拉疫苗的临床试验I阶段,因此它尚未获得第二阶段的批准。从概念上讲,努桑塔拉疫苗也是无效的,数据仍然不完整。
The English, Chinese, Japanese, Arabic, and French versions are automatically generated by the AI. So there may still be inaccuracies in translating, please always see Indonesian as our main language. (system supported by DigitalSiber.id)