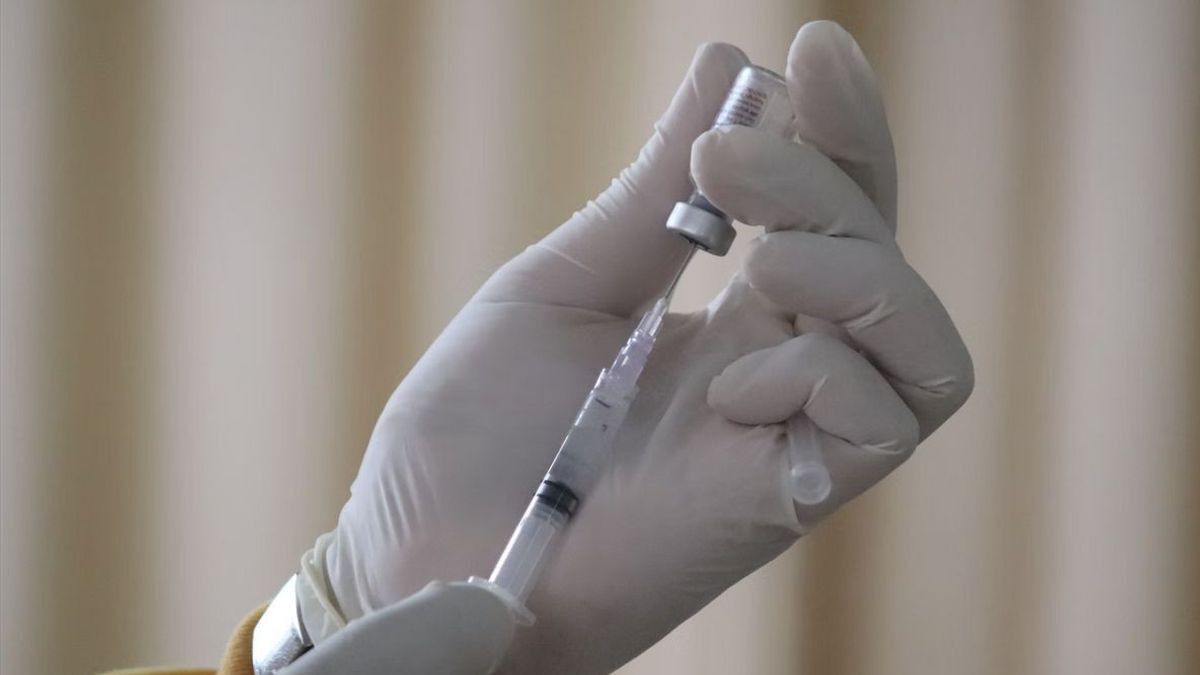
印度尼西亚卫生部发言人Mohammad Syahril博士表示,在印度尼西亚使用Mplax疫苗已获得世卫组织和BPOM的批准,而不是实验性疫苗,因此可以在卫生紧急情况下给予。
Syahril 提到这一点是为了回应声称准备的Mopox疫苗是一种实验性疫苗的叙述。事实上,这一说法伴随着邀请公众拒绝Mopox疫苗。据他说,这一说法是错误的。
「Mopox疫苗已收到世卫组织(世界卫生组织)的紧急使用列表(EUL)和BPOM(食品和药物管理局)的紧急使用授权(EUA),这意味着这种疫苗可以在紧急情况下使用,”Syahril被ANTARA引述,9月12日星期四。
他说,在实施疫苗接种时,全国免疫接种后随访事件委员会(Komnas KIPI)也监测安全性,并确保给予Mapux疫苗的益处,以防止Mapux病毒(MPXV)的传播。
他说,目前,在印度尼西亚使用的Mullax疫苗是一种改良的安卡拉 - 北巴伐利亚北欧疫苗(MVA-BN),这是一种非复制性的第三代天花衍生疫苗(smallpox)。
他说,自2023年以来,在印度尼西亚发现mpax确诊病例后,已经实施了MVA-BN疫苗接种。
他指的是世卫组织于2024年8月23日发布的题为“两周流行病记录:小痘和MPH(正痘病毒)疫苗位置文件”的文件,其中有三种疫苗可用于预防Mopox。
他说,这三种疫苗最初用于天花预防,但后来开发并扩大其用途以预防mpux。
首先,MVA-BN。该疫苗于2013年在加拿大和欧盟获得天花预防批准,针对18岁及以上人群。2019年,MVA-BN被批准用于美国成人天花和mamox预防。
同年,加拿大扩大了MVA-BN以预防mpax。2022年7月22日,欧盟批准了MVA-BN,用于预防成人Mpax。18岁以下的人的MVA-BN未获得许可。
其次,LC16m8。他解释说,在日本,LC16m8于1975年为无年龄限制天花病获得许可,并于2022年8月扩展至Morax预防。使用的LC16m8是第三代天花疫苗。
第三,ACAM2000。Syahril补充说,自2007年以来,第二代天花疫苗已获得美国食品和药物管理局(FDA)的天花免疫接种批准。2024年,根据扩展途径调查新药(扩展途径调查新药)协议,该疫苗被批准预防mpax。
根据2024年9月1日在Taylor&Francis Online上发表的题为“反素疫苗:MVA-BN和LC16m8”的杂志的专家评论,他说,MVA-BN的概率将素疾病降低了62%至85%。在接触过素疫苗的人中,MVA-BN将疾病风险降低了20%。
他补充说,根据临床试验的结果,LC16m8提供了针对mpux病毒的保护。MVA-BN和LC16m8始终如一地发展了对正痘病毒的中性抗体反应,包括Clade I MPXV。
此外,Syahril说,从动物模型研究中获得的ACAM2000功效发现,与未接种疫苗的控制组相比,ACAM2000疫苗对MPXV病毒有效。
The English, Chinese, Japanese, Arabic, and French versions are automatically generated by the AI. So there may still be inaccuracies in translating, please always see Indonesian as our main language. (system supported by DigitalSiber.id)