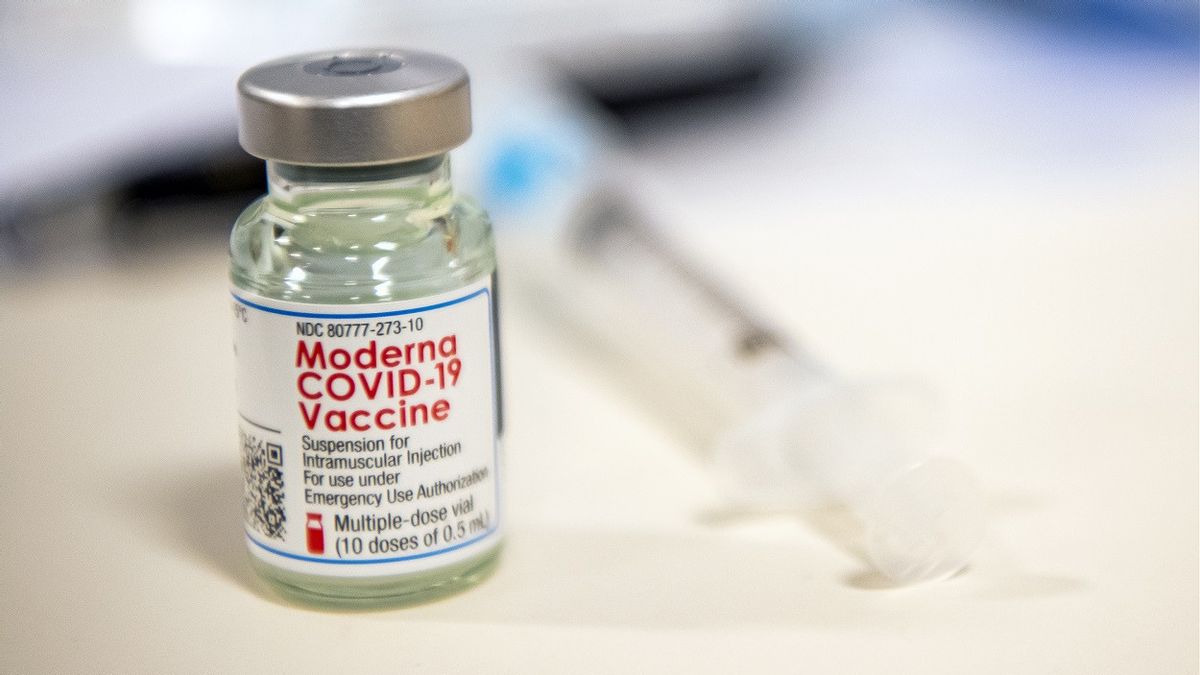
Des scientifiques de la Food and Drug Administration (FDA) des États-Unis ont déclaré mardi que le vaccin de Moderna ne répondait pas à tous les critères de l’agence pour l’utilisation d’une troisième dose ou d’une dose de rappel du vaccin contre la COVID-19, car les deux premières doses sont suffisantes pour faire face à la COVID-19.
Dans un document publié, le personnel de la FDA a déclaré que les données du vaccin de Moderna montraient que la troisième dose du vaccin augmentait effectivement les anticorps protecteurs. Cependant, la différence dans les niveaux d’anticorps avant et après l’injection n’était pas significativement différente, en particulier pour ceux qui avaient des niveaux suffisamment élevés.
Le document a été publié avant une réunion consultative d’experts de la FDA prévue plus tard cette semaine pour discuter de l’administration d’une troisième dose ou d’une dose de rappel du vaccin contre la COVID-19. La FDA suit généralement les conseils de ses experts, mais n’est pas tenue de le faire.
Pendant ce temps, un comité consultatif des Centers for Disease Control and Prevention (CDC) des États-Unis se réunira la semaine prochaine pour discuter de recommandations spécifiques sur les personnes pouvant recevoir des rappels, si la FDA les autorise.
« Il y a une amélioration, bien sûr. Est-ce suffisant pour s’améliorer? Qui sait? Aucune amélioration standard connue n’est nécessaire, et il n’est pas non plus clair dans quelle mesure l’amélioration s’est produite dans cette étude », a déclaré John Moore, professeur de microbiologie et d’immunologie au Weill Cornell Medical College de New York, dans un courrier électronique, citant Reuters le 13 octobre.
Moderna est connu pour demander l’autorisation d’une dose de rappel de 50 microgrammes, soit la moitié de la force du vaccin original administré en deux injections à environ quatre semaines d’intervalle.
La société a demandé aux régulateurs d’éliminer progressivement la vaccination à troisième dose pour les adultes de 65 ans et plus, ainsi que pour les personnes à haut risque, similaire à l’autorisation obtenue par le vaccin à ARNm de Pfizer / BioNTech.
Par ailleurs, le gouvernement des États-Unis sous la présidence de Joe Biden avait précédemment annoncé son intention d’administrer des doses de rappel à la plupart des adultes. Cependant, les scientifiques de la FDA dans un article de la revue « The Lancet » disent qu’il n’y a pas assez de preuves pour soutenir une dose de rappel pour tout le monde.
Les données sur la nécessité d’une dose de rappel du vaccin contre la COVID-19 proviennent principalement d’Israël, qui a lancé une troisième dose de vaccination à l’aide du vaccin de Pfizer pour la majorité de sa population et a fourni des détails sur son efficacité aux conseillers pays de l’Oncle Sam.
Il n’y a pas de population d’étude similaire dans le monde réel pour les vaccins Moderna ou Johnson & Johnson (J & J).
« Les preuves d’augmentation de dose de Modern ont de nombreux défauts », explique le Dr Eric Topol, professeur de médecine moléculaire et directeur du Scripps Research Translation Institute à La Jolla, en Californie, note que les données fournies sont limitées et n’offrent aucun aperçu de la façon dont les boosters fonctionnent réellement chez les humains.
« C’est assez loin de ce que Pfizer a d’Israël, où ils ont une récupération complète de l’efficacité du vaccin à partir du rappel », a déclaré Topol.
À noter, les conseillers de la FDA envisageront également une dose de rappel pour le vaccin à dose unique de J & J vendredi. La FDA n’a pas publié son document d’information sur le tir.
J & J a demandé à la FDA d’autoriser un rappel au moins deux mois après l’injection initiale. Les données ont montré que les adultes à haut risque devraient recevoir des rappels plus tôt, mais que les personnes à faible risque pourraient bénéficier d’attendre au moins six mois pour leur deuxième injection.
The English, Chinese, Japanese, Arabic, and French versions are automatically generated by the AI. So there may still be inaccuracies in translating, please always see Indonesian as our main language. (system supported by DigitalSiber.id)