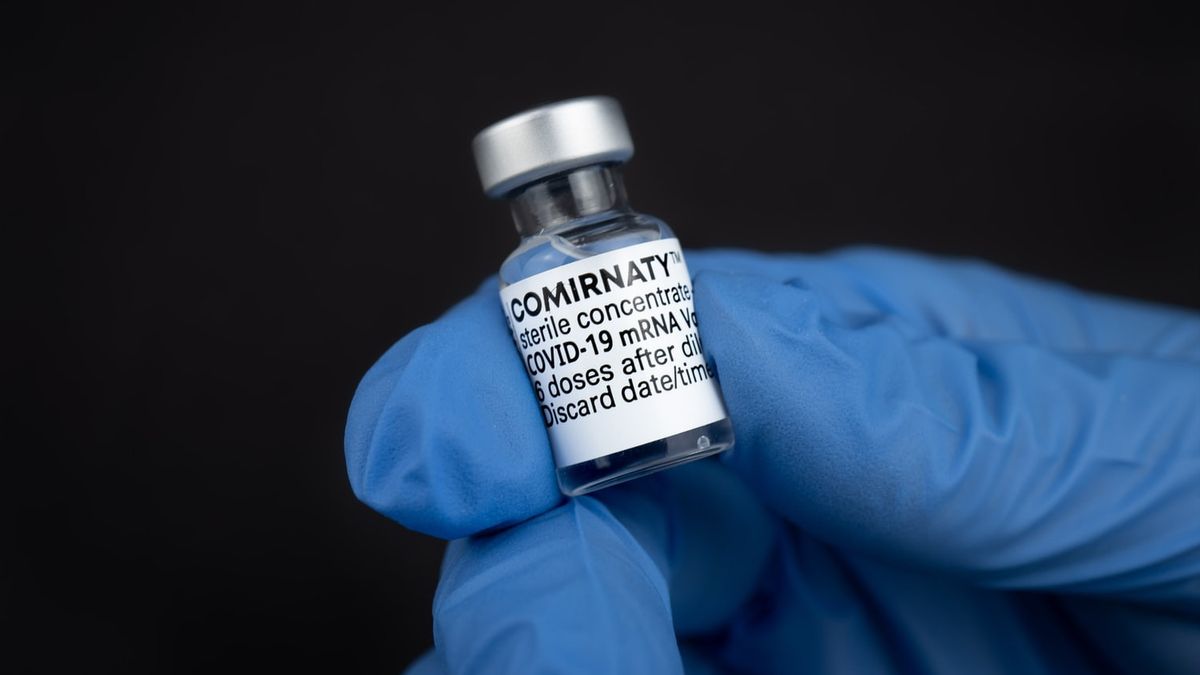
据《华尔街日报》(WSJ)报道,美国 卫生监管机构正在推迟对辉瑞公司针对5岁以下儿童的COVID-19疫苗的审查,因为其两剂方案对Omicron变体无效。
上周,美国食品和药物管理局(FDA)表示,它需要更多关于疫苗的数据,因此决定将疫苗在6个月至4岁的儿童中推迟使用至少 两个月。
数据的初步图片显示,在测试期间,疫苗对Delta变体有效,而Delta成为主要变体。但报告称,一旦Omicron出现,一些接种疫苗的儿童就患有COVID-19,并援引熟悉FDA决定的人士的话说。
但报告称,由于COVID-19病例总体消退,少量的Omicron球衣使疫苗在最初的统计分析中似乎不那么有效。
FDA没有回应路透社的评论。
辉瑞和BioNTech已应FDA的要求于今年2月初提交了三剂方案计划前两剂的数据。辉瑞没有披露功效数据。
该文件令人惊讶,因为在2021年12月,两家公司都表示,低剂量两剂疫苗的初步试验结果并不像想象的那样,临床试验转向测试三剂疫苗。
The English, Chinese, Japanese, Arabic, and French versions are automatically generated by the AI. So there may still be inaccuracies in translating, please always see Indonesian as our main language. (system supported by DigitalSiber.id)