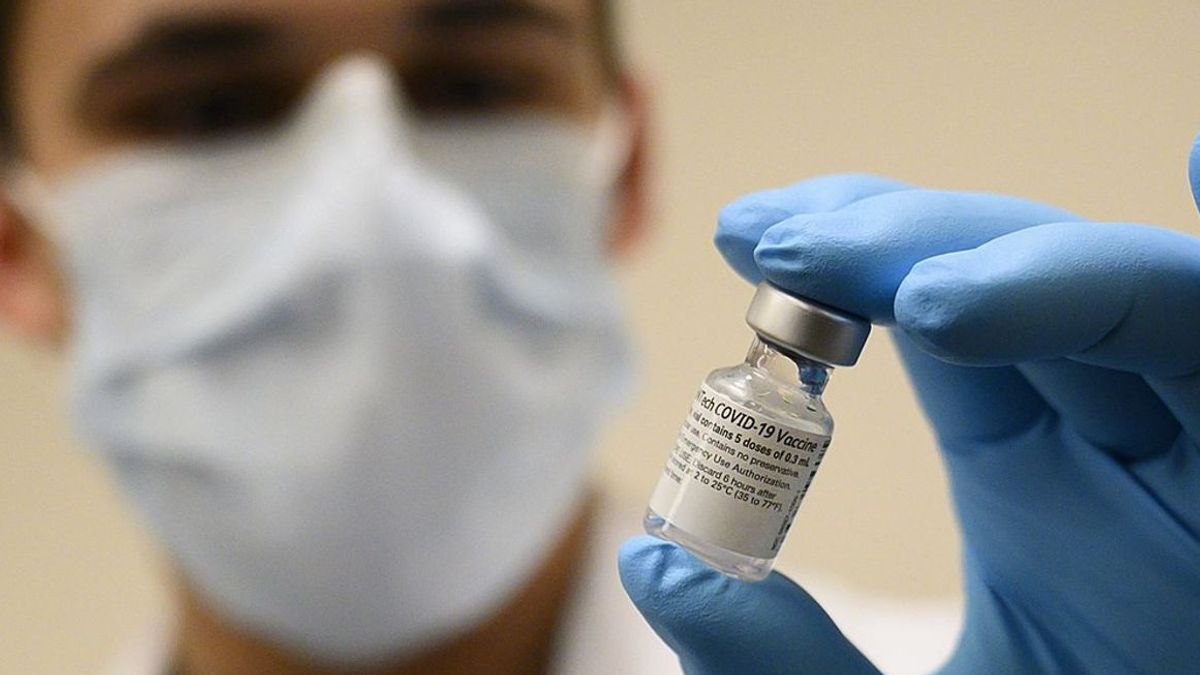
ジャカルタ - 食品医薬品局(BPOM)は、シノヴァック製のCovid-19ワクチンをサンプリングしてテストしています。これには、緊急使用許可(EUA)に従って120万個のワクチンのロットリリース証明書を発行する必要があります。
「空港で受け取る過程で、POM機関は文書の適合性とコロナヴァックワクチン貯蔵エリアの温度適合性をチェックします」と、Covid-19ワクチン接種スポークスマンルチア・リズカ・アンダルシアは1月5日火曜日に公式声明で述べました。
さらに、BPOMはまた、2020年12月31日に来たシノヴァックからCovid-19ワクチンの180万用量のロットリリースを間もなく発行します。ロットリリース証明書は、ワクチンの品質を確保する上で満たさなければならない重要な要件です。
この要件は、世界保健機関(WHO)が設定した標準であり、各ロットまたはワクチンのすべてのバッチの品質を確保するために各国の医薬品当局によって行われる評価プロセスです。
「この証明書の発行のために、POM庁は国立医薬品食品検査開発センターの研究室でテストを行います」と、rizkaが言いました。
ルチアは、このステップはCOVID-19ワクチンEUAの発行を加速するために行われたと説明しました。BPOMが、製薬業界が所有するデータを徐々に提出できるように、ローリング提出を行う場所。
BPOMはまた、ワクチン使用の安全性と免疫応答を評価するために、前臨床試験データ、フェーズ1およびフェーズ2臨床試験を評価しました。BPOMはまた、第3相臨床試験の結果を2回目の注射後1ヶ月以内に監視する。
「もちろん、WHOの要件に従って、中間分析のために少なくとも3ヶ月まで観測を行う必要があります。これは、EUAの提供を支持するデータとしてワクチンの安全性と有効性に関するデータを得るために使用されます」と、彼が結論付けました。
The English, Chinese, Japanese, Arabic, and French versions are automatically generated by the AI. So there may still be inaccuracies in translating, please always see Indonesian as our main language. (system supported by DigitalSiber.id)