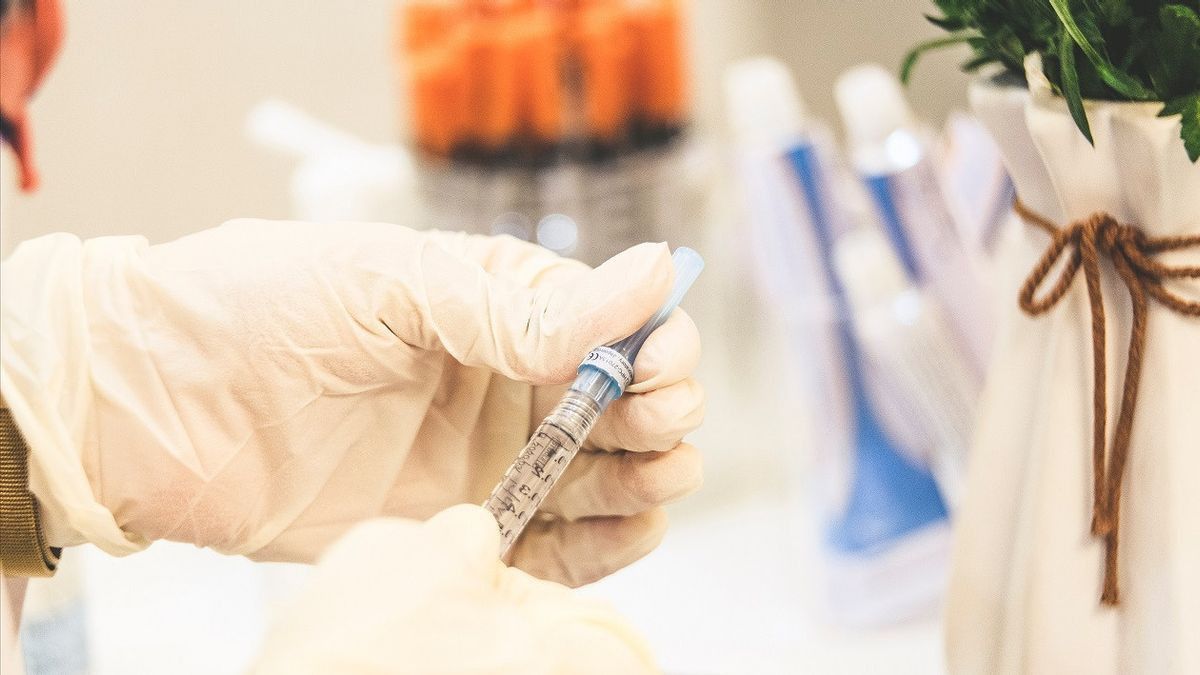
雅加达 - 政府表示支持开发国产COVID-19疫苗,从梅拉普提疫苗到努桑塔拉疫苗。
据乔科维总统说,在仍然困扰着该国的COVID-19大流行中,药物和疫苗的研发非常重要。然而,总统提醒说,疫苗开发过程必须遵循科学原则。
在总统的支持下,国家儿童制造的两种疫苗之间的争论更加明显。此前,前卫生部长特拉万·阿古斯·普特兰托(Terawan Agus Putranto)发起的Nusantara疫苗研究被否决,因为它被认为不符合临床原则。
特拉万必须同意,如果努桑塔拉疫苗许可证被食品和药物监督局(BPOM)停止,并取消政府资助。因为另一方面,梅拉普蒂赫疫苗小组接受了不同的态度,该小组被允许继续其发展。事实上,它肯定会在2022年年中获得紧急使用授权(EUA)。
那么,是什么影响了食品和药物监督机构(BPOM)区分努桑塔拉疫苗和梅拉普提疫苗的态度呢?
努桑塔拉疫苗据说,Nusantara疫苗使用树突方法,与美国加利福尼亚州的AIVITA生物医学公司合作,与PT.拉玛翡翠多苏克斯(拉玛制药公司)合作。这种疫苗开发始于2020年底,当时特拉万·阿古斯·普特兰托还是卫生部长。
在技术方面,使用支离细胞可以根据每个患者的情况生产这种疫苗。因此,这种疫苗声称对合并者或老年人是安全的。先天性细胞技术以前常用于癌症治疗。
印度尼西亚公共卫生专家协会(IAKMI)的健康专家Hermawan Saputra博士透露,即使在美国,这种脱毛方法仍在辩论之中,尚未获准进行测试。
梅拉普提疫苗与此同时,政府已经支持了国家预算的梅拉普蒂赫疫苗,试验将在2022年完成。
Merah Putih疫苗不只指一种疫苗,而是指由研究和技术部/国家研究与创新局(Kemenristek/BRIN)主持的研究财团开发的一组疫苗候选疫苗。
在这个财团中,有7个机构也开发梅拉普提疫苗,每个机构都有不同的平台,其中之一是LBM艾克曼。
努桑塔拉和梅拉普蒂赫疫苗开发阶段
努桑塔拉疫苗的发起人泰拉万·阿古斯·普特兰托说,基于自体支气相突细胞或白血球成分的努桑塔拉疫苗已经通过临床前阶段的动物试验。事实上,他声称这种疫苗使用是安全的。
"我有 WhatsApp 关于美国第三方疫苗安全性 (安全) 和疗效的临床前测试结果。嗯,已经这样做了,所以我们不再在印度尼西亚做(线前测试),"Terawan在联合委员会第九次会议上说。3月12日星期五,雅加达塞纳扬综合体DPR大楼的DPR RI。
"结果已经存在。我们已经把他们送到了英国石油公司。我还与冠状病毒研究和疫苗配方小组组长查鲁尔·尼多姆·安瓦尔教授就努桑塔拉疫苗的突起细胞临床前测试进行了咨询,"他继续说。
与此同时,新型冠状病毒梅拉普提疫苗的研制工作已进入动物试验的准备阶段。
艾克曼分子生物学研究所所长阿明·索班德里奥说,他的政党目前正在从哺乳动物细胞表达系统和酵母细胞中收集重组蛋白。
这两个细胞将用作一种重组蛋白工厂。如果重组蛋白的生产是恒定的,那么继续进行动物试验。
此外,阿明解释说,他的机构自去年3月以来有12个月的时间获得疫苗种子。疫苗种子将作为生产者交给生物法玛。
他补充说,在批量生产之前,Bio Farma必须进行临床试验阶段1至3,并从食品和药物监督局(BPOM)获得分销许可证。
考虑到梅拉普提疫苗的发展取自印度尼西亚传播的病毒,它比国外的疫苗更有效、更安全吗?阿明说,他无法比较,因为还没有数据。
"如果它是安全的,我们将确保,是的。我们也不急于工作,因为我们确保安全。如果它有效,我们无法将其与其他疫苗进行比较,因为目前还没有数据,"Amin 说。
政府对努桑塔拉疫苗和梅拉普提疫苗的态度
食品和药物监督局(BPOM)负责人佩妮·卢基托说,她的机构正在协助国产梅拉普提疫苗的研制过程。
Merah Putih 疫苗的开发计划于 2020 年 3 月至 2021 年 2 月进行,从抗原识别、病毒种子制作和疫苗原型开始。
Penny 说:"这种疫苗原型将提交给 Biofarma,以进行下游流程,包括升级、临床前测试、第 1、2 和 3 阶段的临床试验,并在 20 个工作日内获得商业化许可。
与此同时,生物法马部长班邦·赫里扬托说,据估计,到2022年年中,印度尼西亚将接种这种梅拉普提疫苗。
班邦还说,研究和技术部和卫生部以前已同意将预算任务与努桑塔拉疫苗分开。
研究和技术部为疫苗种子和基础设施提供了预算,而临床试验预算在卫生部。
"我们已准备好适应,但事实上,Nusantara疫苗阶段已进入临床试验阶段。虽然我们大多在上游,在实验室,"班邦说。
同时,临床试验小组的目标是,从2021年6月起,Nusantara疫苗可以批量生产。但是,只有当食品和药物监督局 (BPOM) 为批准在未来两个月内实施临床试验 II 和 III 的临床试验 (PPUK) 开绿灯时,才能实现此情况。
后来,由前卫生部长特拉万·阿古斯·普特兰托发起的疫苗将需要180名志愿者进行II.临床试验。同时,第三阶段临床试验需要1,600名志愿者。
因此,可以得出结论,实际的梅拉普提疫苗生产将在2021年底或2022年初由生物法马开始。
至于努桑塔拉疫苗,这是由博士开发的。Terawan和合作伙伴,他们的发展被食品和药物监督局(BPOM)拒绝,理由是他们不符合良好的临床原则。
The English, Chinese, Japanese, Arabic, and French versions are automatically generated by the AI. So there may still be inaccuracies in translating, please always see Indonesian as our main language. (system supported by DigitalSiber.id)