雅加达 - 食品和药物监督局(BPOM)颁发了使用国产InaVac疫苗的许可证,用于疫苗接种剂量1和2或初级疫苗
BPOM RI Penny K Lukito负责人今天(11月4日星期五)表示,宣布了由PT Biotis制药印度尼西亚生产的InaVac疫苗的紧急使用授权(EUA)。
佩妮说:“今天,BPOM非常感激地宣布批准以InaVac的名义使用国产COVID-19疫苗的EUA,作为红白疫苗之一。
他说,灭活病毒疫苗是由Airlangga或Unair的研究人员开发的,由PT Biotis在位于西爪哇茂物摄政区辛杜尔山的生产设施中生产。
InaVac 初级疫苗被批准用于刺激人体对 SARS-CoV-2 的免疫力,以预防 18 岁及以上人群的 COVID-19。
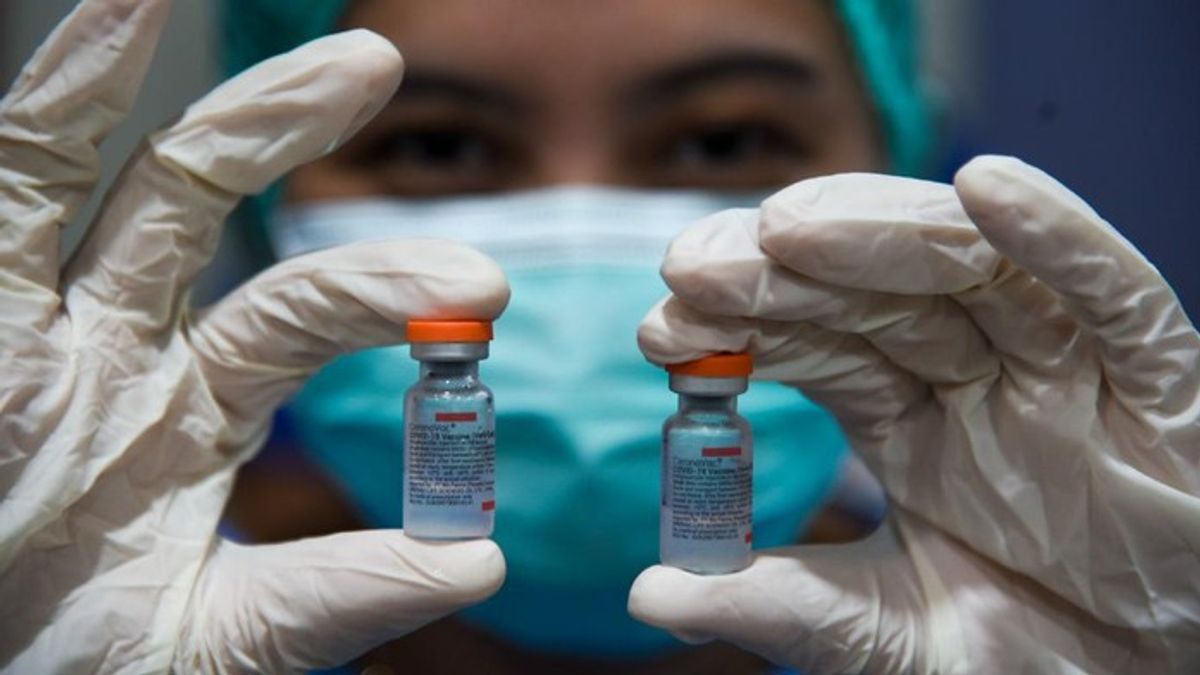
该疫苗每针间隔注射两剂,持续28天,效力相当于CoronaVac疫苗。
根据Penny的说法,InaVac疫苗已经用许多最新的冠状病毒变种进行了测试。
他说:“制药行业一直致力于满足质量要求,并代表PT Biotis批准了InaVac疫苗EUA进行初级疫苗接种,它已开始支持国内COVID-19疫苗的独立性。
BPOM感谢国家COVID-19疫苗评估委员会专家组和印度尼西亚免疫技术咨询小组(ITAGI)在研究供公众使用的InaVac疫苗方面的合作。
根据Penny的说法,InaVac初级疫苗的生产已经在进行中,并将在不久的将来与首次向公众使用。
他说:“分发过程在卫生部进行,因为政府将购买和采购InaVac疫苗。
在同一活动中,Unair研究员费迪克斯·阿卜杜勒·兰塔姆教授表示,InaVac对SARS-CoV-2最新变种的初步剂量测试结果具有良好的能力和高度的保护作用。
“我们相信这种疫苗具有良好的能力,可以从病毒开始到最晚的感染中和,”他说。
根据Fedix的说法,最新的变种,即XBB和XBC,症状轻微。“通过使用恶性Delta变体中和测试进行比较,结果很好,”他说。
PT Biotis Pharmaceutical Indonesia FX Sudirman董事表示,到2022年底,InaVac初级剂量阶段的产量达到500万剂。
他总结说:“卫生部在2022年11月的期望必须是可用的,因为该国的疫苗库存目前有限。
The English, Chinese, Japanese, Arabic, and French versions are automatically generated by the AI. So there may still be inaccuracies in translating, please always see Indonesian as our main language. (system supported by DigitalSiber.id)