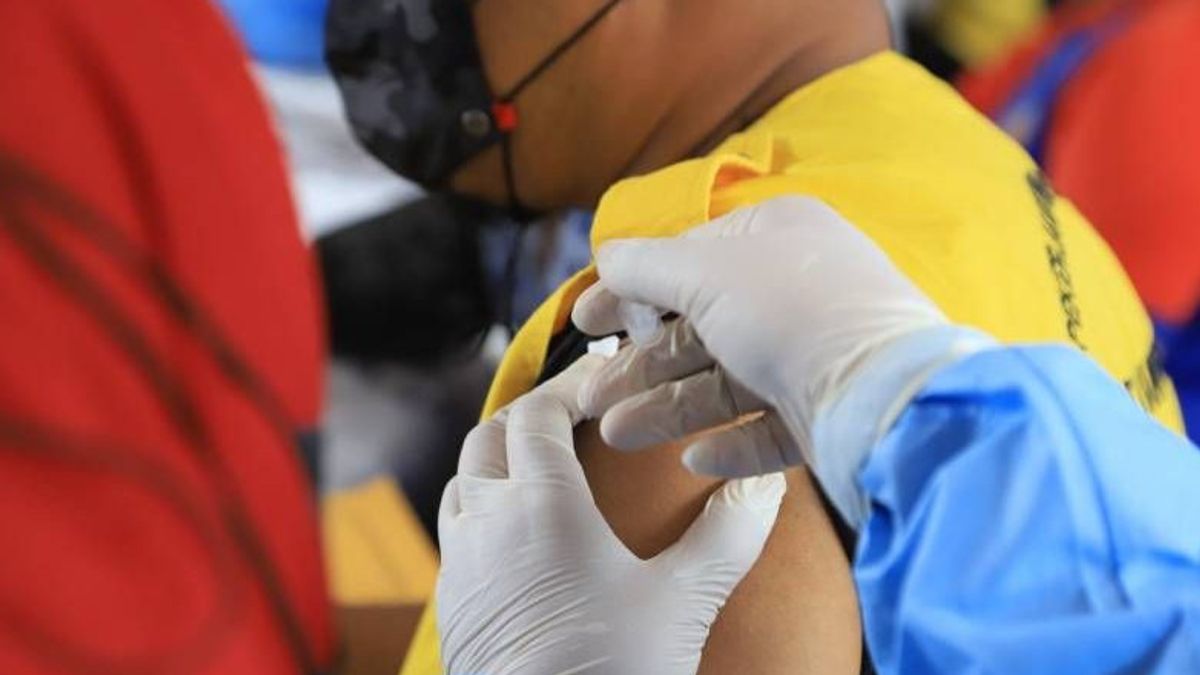
ジャカルタ - 食品医薬品局(BPOM)によって赤と白のワクチンに与えられた臨床試験許可は、COVID-19パンデミックに対処するインドネシアにとって大きな一歩です。これは疫学グリフィス大学、オーストラリアディッキーブディマンによって述べられています。
「赤と白のワクチンは重要です。「COVID-19パンデミックに対応する意味で短期的なだけでなく、長期的にも」と、彼はジャカルタでアンタラが2月12日(土曜日)に受け取った音声メッセージで言いました。
彼は、インドネシアはすでにPTを持っているにもかかわらず、述べました。バイオファーマはワクチンを生産し、最初から本当に始まったワクチン検査の研究は、ワクチン研究を行うことができる国のランクに入る国の大きな基盤です。コミュニティのためのワクチンの入手可能性または在庫を国が独立して生産するのを支援することを含む。
「生産能力は明らかにそこにあるが、"研究開発"によるワクチン研究は容易ではない利点である。それは投資を必要とし、長い時間がかかります。「このような研究だけでも、実際には私たちにとって非常に高度なステップです」とDicky氏は述べています。
彼によると、感染症のワクチンを研究することについて話すとき、成功の可能性は50〜50です。ワクチンが様々な一連のテストに合格することができれば、州は一般に配布されることを疑う必要のないページで独自にワクチンを生産することができます。
各国はまた、COVID-19ワクチンに対応して心理社会的およびコミュニティ行動を変えることもできます。しかし、それが失敗した場合、赤と白のワクチンは、将来の研究のための非常に貴重な経験になります。
「他の人がうまくいかないとしても、少なくともその研究にとって非常に貴重な経験になる可能性があります。失敗は次の段階に到達するための良い基盤です」と、彼が言いました。
国の子供たちの深刻さを見て、彼は政府が行われている研究に支援を提供することに本当に真剣であることを願っています。なぜなら、ワクチン検査は、状況が発生したとき、またはパンデミック状態が政府によって取り消されたときにはっきりと見えるからです。さらに、この研究の成功は、COVID-19が最後のパンデミックまたはオミクロンを最後の変異体としてではないことを考慮する際にも重要である。
「もう一度、赤と白のワクチンの研究は、確かに世界的な国際基準でもある基準でサポートされ続ける必要があります」と、ディッキー・ブディマンが言いました。
これとは別に、食品医薬品局(BPOM)のペニー・K・ルキト長官は、第1段階と第2相における赤と白のワクチン臨床試験の実施には、フェーズ1とフェーズ2の405人のボランティアが含まれていると述べた。
第1相および第2相臨床試験が中間結果を得て適格である場合、第3段階の臨床試験に進むことができます。
「第3相臨床試験の中間結果を得た後、POM庁に提出し、2022年7月中旬頃の緊急使用許可(EUA)の承認を得ることができます」と、ペニーは2月7日(月曜日)にジャカルタで記者会見しました。
彼は、この臨床試験で与えられる赤と白のワクチンの品質は、医薬品の良い方法(CPOB)の要件を満たすPTバイオティス医薬品インドネシアの生産施設によって満たされ、サポートされていることを強調しました。
Merah Putihワクチンのメーカーであるペニー・K・ルキト氏によると、商業規模で使用されるワクチン生産の規模を増やすことで、第3相臨床試験の準備を並行して行った。
The English, Chinese, Japanese, Arabic, and French versions are automatically generated by the AI. So there may still be inaccuracies in translating, please always see Indonesian as our main language. (system supported by DigitalSiber.id)