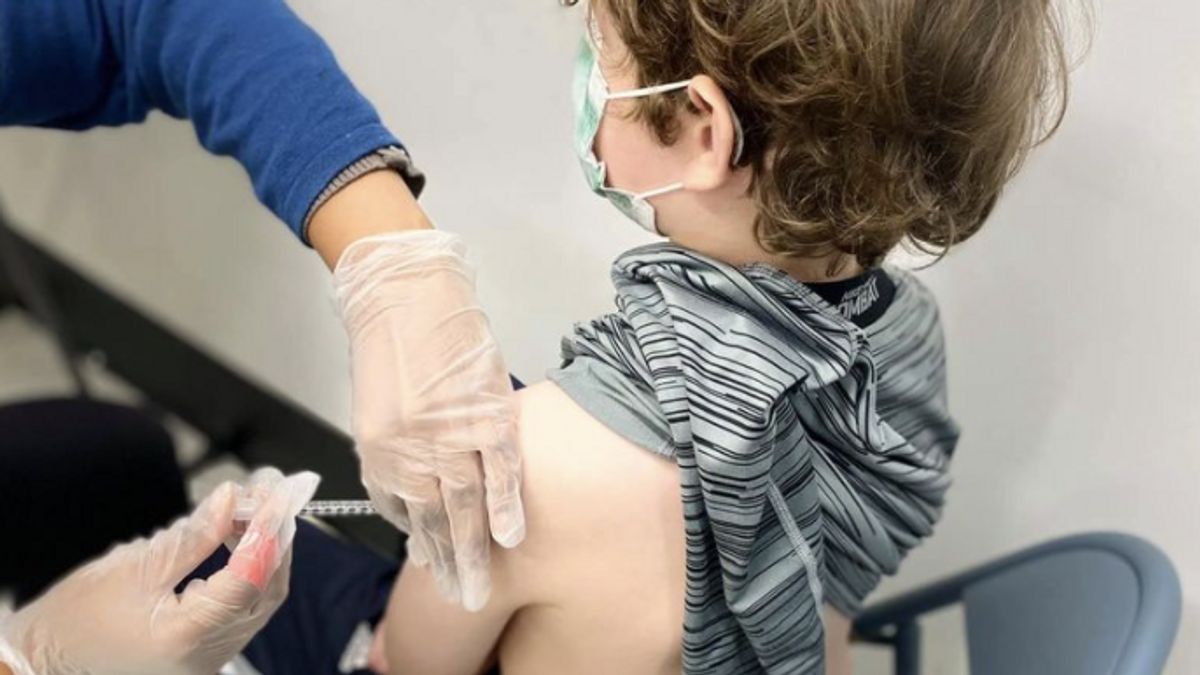
米国疾病予防管理センター(CDC)の文書によると、米国政府は早ければ2月21日に5歳未満の子供に対してCOVID-19ワクチン接種を開始する予定です。
米国食品医薬品局(FDA)は、2~4年間の臨床試験で主要な目標を達成していないにもかかわらず、ファイザー社のワクチンとBioNTech SEを年齢層で使用することを許可することを検討しています。
製薬会社は、彼らが年齢層の緊急の公衆衛生ニーズに対処するためにFDAの要求で承認を支持するデータを提出したと言いました。
FDAの外部弁護士は2月15日に会合を開き、規制当局にワクチンの承認を勧告するかどうかを議論する予定です。まだショットの対象外ではない唯一の年齢層である5歳未満の子供のためのワクチンの発売は、会議の1週間以内に開始されます。

CDC文書によると、米国政府は、FDAが使用を許可する場合、2月末までにファイザー/BioNTechワクチンの最初の1000万回の用量を州やその他の団体に出荷する計画です。
米国には6ヶ月から4歳までの合計で約1,800万人の子供がいて、最初の1000万回を超える追加の物資があるだろう、とCDCは述べた。
2月21日に始まる最初の打ち上げは、子供たちが重篤なCOVID-19病のリスクが高い地域を優先します。
その後、連邦薬局の管轄区域とパートナーは、CDCの勧告から約1週間後の2月23日と2月25日に2回目と3回目の用量の配達を受け取ります。
ディケタヒの場合、この年齢層の子供は、許可されれば、ワクチンのより低い用量を受け取る。ファイザー/バイオンテックは、5歳から11歳までの小児で10マイクログラム、12歳以上の30マイクログラムの用量と比較して、年齢層でワクチンの3マイクログラム用量をテストした。
The English, Chinese, Japanese, Arabic, and French versions are automatically generated by the AI. So there may still be inaccuracies in translating, please always see Indonesian as our main language. (system supported by DigitalSiber.id)