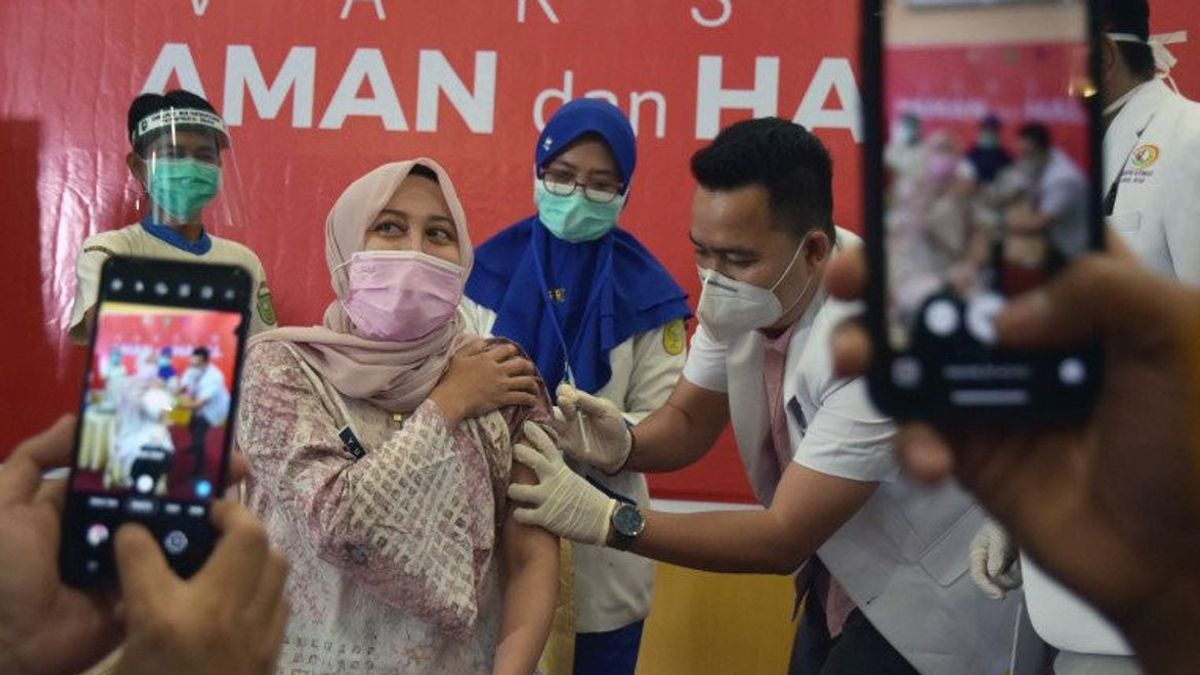
JAKARTA - La Food and Drug Administration (BPOM) a décidé de retarder l’utilisation du vaccin astrazeneca suite à l’émergence de cas de patients en coagulation du sang dans plusieurs pays.
BPOM a déclaré que la décision sur le délai attend la confirmation de l’Organisation mondiale de la Santé (OMS) et du Groupe consultatif stratégique d’experts sur la vaccination (SAGE) concernant l’innocuité des vaccins en provenance du Royaume-Uni.
« J’espère que dans un délai pas trop long », a déclaré penny K Lukito, chef de bpom, lors d’une réunion de travail avec la Commission IX dvr, lundi 15 mars.
Il a révélé qu’il avait déjà un dossier (dossier) de l’OMS concernant le vaccin Astrazeneca, afin qu’il puisse le savoir jusqu’à la question de l’innocuité du vaccin.
Penny a également confirmé que le numéro de lot d’Astrazeneca avait suspendu son utilisation dans un certain nombre de pays de l’Union européenne (UE), contrairement aux numéros de lots d’astrazeneca entrant en Indonésie par des canaux multilatéraux.
« Toutefois, par prudence, nous sommes toujours en train de communiquer avec l’OMS et le SAGE. Les résultats de la communication seront discutés par les équipes interse sectorielles et le ministère de la Santé pour la prise de décision sur l’utilisation d’Astrazeneca dans le programme national de vaccination », a déclaré Penny.
BPOM a procédé à une évaluation approfondie du vaccin astrazeneca. Il a mentionné que le vaccin Astrazeneca est entré en Indonésie par deux voies, le régime multilatéral du Fonds GAVI/Covax et le régime bilatéral.
Pour les canaux multilatéraux, a déclaré Penny, le vaccin Astrazeneca reçu par l’Indonésie a reçu une liste d’utilisation d’urgence (EUL) suivie d’une autorisation d’utilisation d’urgence (EUA) de l’OMS.
Penny a expliqué que l’OMS avait initialement donné l’EUL, mais BPOM n’a pas immédiatement accepté et a exhorté l’agence des Nations Unies pour la santé à continuer à fournir l’EUO.
BPOM, a-t-il poursuivi, a communiqué et exhorté à fournir aux Émirats arabes unis afin qu’ils obèrent enfin un accord de confidentialité lié au dossier vaccinal.
« Avec l’accord de confidentialité, nous avons procédé à une évaluation approfondie comme d’autres vaccins, mais nous n’avons donné l’autorisation d’utilisation d’urgence que le 22 février 2021 », a déclaré Penny.
Plus tôt dans la même réunion, le ministre de la Santé Budi Gunadi Sadikin a déclaré qu’il retardait l’utilisation du vaccin COVID-19 d’AstraZeneca en Indonésie en attendant les résultats d’une étude de l’Organisation mondiale de la Santé (OMS).
À l’heure actuelle, a déclaré Budi, l’OMS et l’Agence de réglementation des médicaments et des produits de santé (Royaume-Uni) et l’Autorité médicale européenne examinent un certain nombre d’effets secondaires tels que la coagulation du sang dans le cas de l’utilisation du vaccin fabriqué à Oxford.
« Jusqu’à présent, l’OMS est toujours à la recherche, nous avons également reçu de la MHRA son BPOM UK, et l’EMA est l’Autorité médicale européenne, ils n’ont pas encore confirmé s’il s’agit d’une corrélation à cause des vaccins ou non », a déclaré Budi Gunadi.
Jusqu’à présent, a déclaré le ministre de la Santé Budi, l’information sur certains cas de coagulation du sang n’est pas causée par le vaccin astrazeneca, mais par d’autres événements. Toutefois, le ministère de la Santé et la Food and Drug Administration (BPOM) ont convenu de déclarer une suspension temporaire de l’utilisation d’AstraZeneca.
« Pour le conservatisme BPOM retardé la mise en œuvre d’AstraZeneca en attendant la confirmation de qui, espérons-le dans un court laps de temps peut sortir, parce qu’il ya une période expirée à la fin du mois de mai, at-il dit.
The English, Chinese, Japanese, Arabic, and French versions are automatically generated by the AI. So there may still be inaccuracies in translating, please always see Indonesian as our main language. (system supported by DigitalSiber.id)